Эхокардиография и источники эмболии (часть 3)
Эффект спонтанного эхоконтрастирования левого предсердия на эхокардиографии
Термин «спонтанныое эхоконтрастирование» (СЭК) или «дым» был придуман при появлении чреспищеводной эхокардиографии (ЧПЭХоКГ) закрученных «дымоподобных» плотных эхосигналов внутри сердца, чаще всего в пределах левого предсердия (ЛП) и, в частности, его ушка (УЛП). СЭК может быть оценена на трансторакальной эхокардиографии, но гораздо лучше видена на ЧПЭхоКГ. Это маркер застоя, отражающий состояния низкого потока и, вероятно, отражающий агрегацию клеток крови при низких скоростях кровотока. Спонтанное эхоконтрастирование на эхокардиографии также является вероятным предшественником тромба. Это наиболее частая находка ЧПЭхоКГ среди пациентов, направленных для оценки возможного сердечного источника эмболии, особенно у пациентов с фибрилляцией предсердий или увеличением левого предсердия. СЭК лучше всего воспринимается при более высоких настройках усиления и может отличаться от фонового «шума» по его вихревому движению. Зависимость данного эффекта от настроек датчика затрудняет количественную оценку; тем не менее, его обычно можно разделить на группы легкой и тяжелой степени. Термин «осадок ушка левого предсердия» был придуман для тяжелого вязкого СЭК без явного тромбообразования, хотя часто бывает трудно провести различие между ними. Считается, что он представляет собой следующий этап в континууме по направлению к образованию тромба, и было высказано предположение, что он имеет большее прогностическое значение, чем СЭК. Недавние данные показали, что осадок ушка левого предсердия на эхокардиографии независимо связан с последующими тромбоэмболическими событиями и смертностью от всех причин у пациентов с фибрилляцией предсердий.
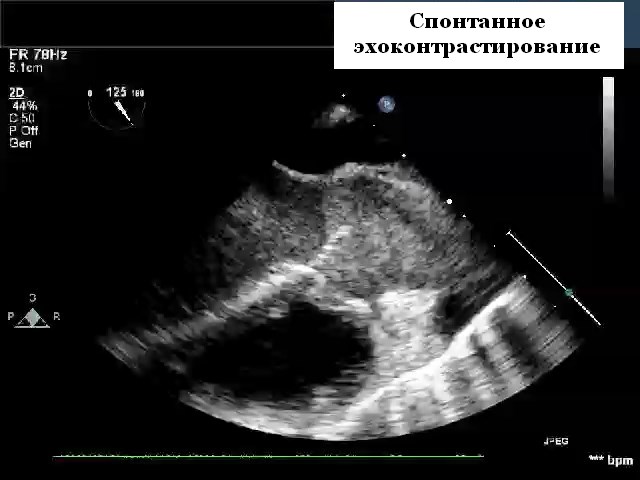
Спонтанное эхоконтрастирование на ЭхоКГ и тромбоэмболия
Существует сильная связь между СЭК и тромбом ЛП. Наличие спонтанного эхокантрастирования является независимым предиктором тромбоэмболического риска; а у пациентов с фибрилляцией предсердий это связано с увеличением частоты эмболии с 3 до 12% в год. Митральная регургитация связана со снижением частоты СЭК, поскольку, предположительно, регургитация «размывает» ЛП, предотвращая застой. Эффект гораздо реже встречается на эхокардиографии у пациентов с синусовым ритмом (2% в одной большой серии, все из которых имели увеличение ЛП), чем у пациентов с фибрилляцией предсердий (распространенность 20% в одной серии), но все же ассоциируется с более высокой частотой встречаемости инсульта. В настоящее время нет единого мнения о лечении СЭК при отсутствии определенного тромба ЛП или фибрилляции предсердий, хотя его наличие требует всестороннего исследования левого предсердия на предмет возможного тромба.
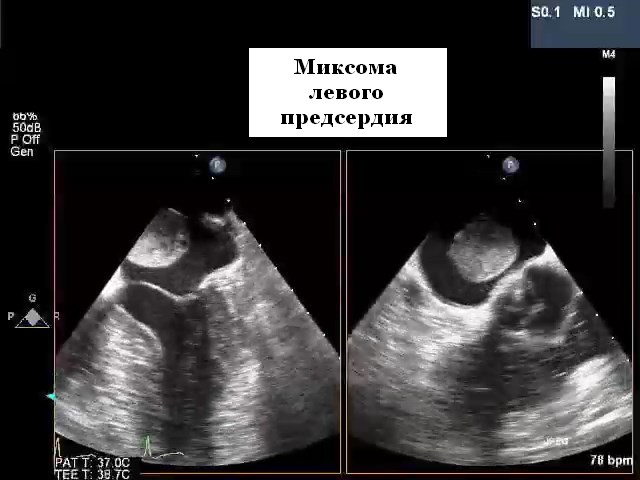
Опухоли левого предсердия на эхокардиографии
Первичные опухоли сердца редки, их частота составляет 0,002–0,03% при вскрытии, при этом миксомы составляют до 50% всех первичных опухолей и более 80% опухолей ЛП. Метастатические опухоли редко распространяются в ЛП и могут имитировать миксому предсердий. Миксомы левого предсердия на эхокардиографии — это обычные опухоли, связанные с эмболическими событиями, хотя любая левосторонняя опухоль может вызывать эмболические осложнения либо из-за эмболии самих фрагментов опухоли, либо из-за эмболизации фрагментов тромба, которые образуются на поверхности опухоли.
Миксома левого предсердия на ЭхоКГ
Эти доброкачественные опухоли чаще встречаются у женщин, их средний возраст составляет 56 лет. Морфологически они выглядят как студенистая рыхлая масса, которая чаще всего возникает на ножке от межпредсердной перегородки в области овальной ямки. Они различаются по размеру, но часто не обнаруживаются, пока не станут очень большими, и к этому времени на эхокардиографии они могут пролабировать через митральный клапан во время диастолы. С эхокардиографической точки зрения они обычно выглядят как подвижные, четко очерченные, негомогенные образования, которые могут содержать кистоподобные структуры и / или области кальцификации. Обычно их можно идентифицировать по трансторакальной ЭхоКГ, однако ЧПЭхоКГ часто требуется для всесторонней визуализации опухоли и помощи в планировании хирургического вмешательства. Важно исключить наличие множественных образований, подтвердить место прикрепления и убедиться, что митральный клапан выглядит нормально. Миксому следует отличать от большого тромба ЛП, хотя последние обычно прикрепляются к задней стенке и имеют многослойный вид. С клинической точки зрения эмболическое событие (часто на нескольких сосудистых бассейнах) является первоначальным проявлением у одной трети пациентов. Другие проявления включают симптомы, связанные с обструкцией митрального клапана или системные конституциональные симптомы (лихорадка, потеря веса). После обнаружения миксома должна быть удалена хирургическим путем. Долгосрочная перспектива отличная, хотя у 5% может возникнуть рецидив, особенно у пациентов с семейной формой.
Тромб левого желудочка на эхокардиографии
Тромб в левом желудочке (ЛЖ) на эхокардиографии обычно возникает в условиях выраженной регионарной систолической дисфункции после острого инфаркта миокарда (ОИМ), чаще после крупных передне-апикальных инфарктов, особенно при наличии признаков формирования аневризмы ЛЖ. Хотя реже, тромб также может образовываться (обычно на верхушке) у пациентов с дилатационной кардиомиопатией и тяжелой глобальной систолической дисфункцией ЛЖ. Современные отчеты предполагают, что тромб левого желудочка развивается примерно у 5% пациентов с ОИМ (~ 12% у пациентов с инфарктами передней стенки), которые получают тромболизис, частота, которая значительно ниже, чем в дотромболитическую эпоху (~ 20%). Большинство тромбов ЛЖ, выявленных на эхокардиографии, развиваются в течение первых 2 недель после ОИМ (в среднем 9,5 дней). Те, у кого тромб развивается рано (в течение 48–72 часов после инфаркта), имеют очень плохой прогноз, поскольку умирают от осложнений, связанных с размером инфаркта, а не от эмболических осложнений. Застой на обширных участках инфаркта и, возможно, воспаление эндокарда во время острой фазы инфаркта, обеспечивающее тромбогенную поверхность, предполагаются в качестве основных патофизиологических факторов.
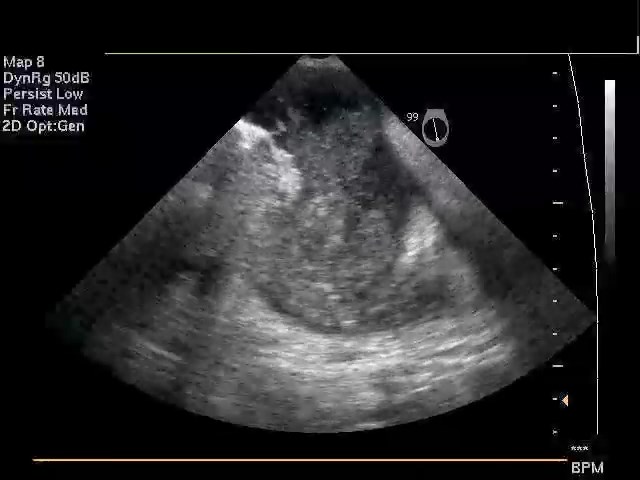
Эхокардиографическая идентификация тромбов сердца
Тромб ЛЖ лучше виден при трансторакальной эхокардиографии, чем при чреспищеводной. Ранее сообщалось о высокой чувствительности (95%) и специфичности (90%) ЭхоКГ для выявления тромба ЛЖ; однако более поздние исследования предполагают чувствительность менее 50% по сравнению с МРТ с контрастным усилением и / или хирургическим подтверждением. Чреспищеводная эхокардиография не является предпочтительным тестом, поскольку обычно трудно визуализировать истинную верхушку, что затрудняет исключение апикального тромба. Обычно тромб ЛЖ проявляется в виде отчетливых эхосигналов в верхушке ЛЖ, которая видна на протяжении сердечного цикла, по крайней мере, на двух разных эхокардиографических позициях. Он может иметь неровную поверхность и может быть сидячим или на ножке, подвижным или плоским. Поэтому нужна адекватная визуализация верхушки ЛЖ у всех пациентов с апикальной дисфункцией ЛЖ для предотвращения пропуска небольших тромбов, которые могут появляться не на всех ультразвуковых срезах.
Используя современные многочастотные преобразователи, следует увеличить апикальную область, максимизировать частоту для оптимизации разрешения в ближнем поле, а фокус отрегулировать по направлению к верхушке ЛЖ. Если есть неуверенность в отношении апикального тромба ЛЖ, заполнение области цветными допплеровскими сигналами низкой скорости (уменьшение предела Найквиста) позволит определить цвет верхушки ЛЖ и может помочь лучше определить, есть ли дефект апикального наполнения (потока). Кроме того, можно и нужно использовать внутривенные контрастные вещества для затемнения верхушки ЛЖ и подтверждения любых аномалий апикального наполнения, если есть сомнения. Последние данные показали, что при контрастировании стромальные опухоли и тромбы выглядят гипоусиленными, в то время как злокачественные и сосудистые опухоли становятся гиперусиленными по сравнению с соседним миокардом.
Риск эмболизации при выявлении тромбов на эхокардиографии
По имеющимся данным, риск системной эмболизации тромбом ЛЖ достигает 10%. Риск наиболее высок в первые 3 месяца после инфаркта, после чего тромб становится организованным, и вероятность его эмболии снижается. Пожилой возраст, более низкая фракция выброса и отсутствие в лечении антитромботических средств или антикоагулянтов независимо связаны с повышенным риском эмболии и инсульта. Также более крупные, выступающие и подвижные тромбы более склонны к эмболии. Предполагается, что наличие смежных зон акинезии и гиперкинезии увеличивает риск эмболии. Эти пациенты с систолической дисфункцией ЛЖ, независимо от того, имеют ли они синусовый ритм или фибрилляцию предсердий, также имеют повышенный риск образования тромба в ушке левого предсердия. Все пациенты с тромбом ЛЖ должны получать антикоагулянты от 3 месяцев до 1 года. В настоящее время как европейские, так и американские согласованные руководства не рекомендуют рутинную антикоагулянтную терапию для пациентов (как с ишемическими, так и с неишемическими) с тяжелой дисфункцией ЛЖ, если нет эхокардиографических доказательств тромба ЛЖ, фибрилляции предсердий в анамнезе или других показаний к антикоагуляции.
