Субаортальный стеноз на эхокардиографии
Обструкция путей оттока левого желудочка (ОПОЛЖ) — это общий термин, используемый для описания серии стенотических поражений, начинающихся в анатомическом тракте оттока левого желудочка и заканчивающихся нисходящей грудной аортой. Эти стенозы, которые часто выявляют на эхокардиографии, могут возникать по отдельности или в комбинации, и все они создают повышенную постнагрузку на левый желудочек. Степень стеноза может быть разной, в легкой форме он хорошо переносится. Однако если обструкция серьезная и не лечится, левый желудочек гипертрофируется и становится менее податливым (диастолическая дисфункция), что может привести к расширению желудочка и систолической недостаточности.
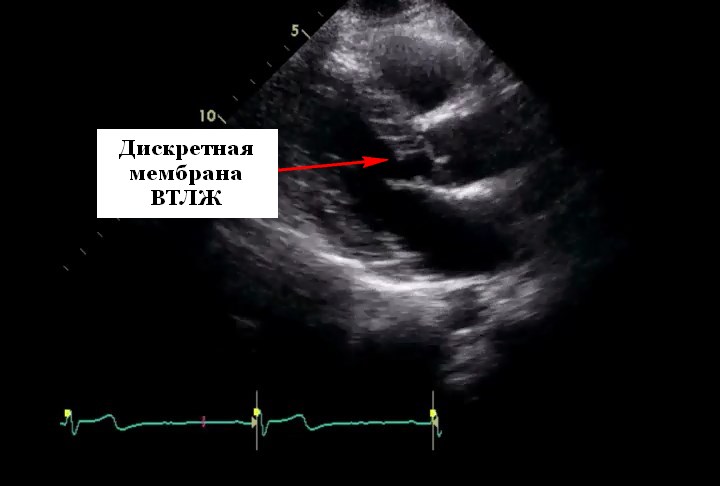
На эхокардиографии обструкция может быть ниже аортального клапана (АК), на уровне клапана, в восходящей аорте, дуге или нисходящей грудной аорте. Подавляющее большинство неклапанных обструкций ЛЖ имеют врожденную этиологию, и стеноз аортального клапана также чаще всего имеет врожденную этиологию у пациентов в возрасте до 50 лет. Трансторакальная эхокардиография с допплерографией является современным краеугольным камнем диагностической оценки пациентов с подозрением на ОПОЛЖ. В данной статье будет проведен современный обзор клинических особенностей обструкции путей оттока левого желудочка и роли эхокардиографии в оценке взрослых с врожденным ОПОЛЖ. В статье мы не будем касаться наследственных аортопатий, гипертрофической кардиомиопатии или приобретенных пороков аортального клапан и самой аорты.
Субаортальный стеноз. Распространенность субаортального стеноза (САС) у взрослых с врожденными пороками сердца составляет около 6,5% при соотношении мужчин и женщин 2: 1. САС может быть дискретным, как в случае фиброзной оболочки, или диффузным, как в случае мышечного сужения выходного тракта левого желудочка, образуя диффузно суженный туннель. Редко аномальные дополнительные митральные хорды, прикрепленные к основанию межжелудочковой перегородки и хорошо видимые на эхокардиографии, могут вызывать субаортальный стеноз.
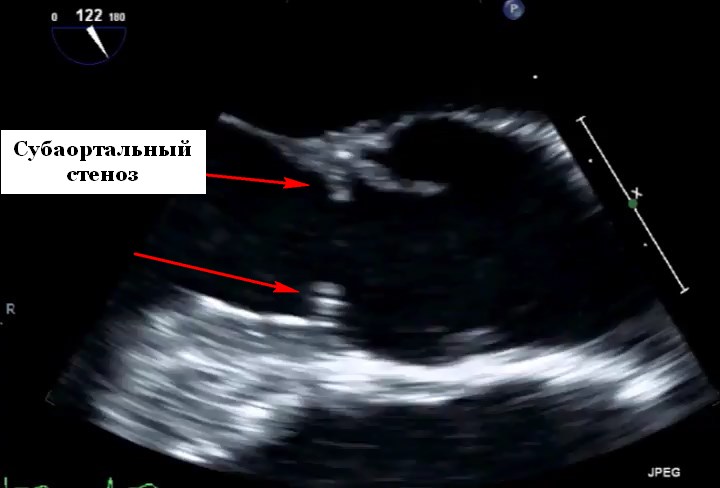
Подавляющее большинство САС относится к дискретному мембранному типу. Расстояние между митральным и аортальным клапаном у пациентов с САС постоянно увеличивается. Было предположено, что изменение направления кровотока около гребня перегородки приводит к дифференцировке эмбриональных клеток в фибробласты, которые образуют «мембрану» ниже аортального клапана. Сопутствующий двустворчатый аортальный клапан (ДАК) присутствует у 23% пациентов, и другие обструктивные поражения также могут сосуществовать. Пациенты с комплексом Шона могут иметь одновременно митральный стеноз и коарктацию аорты (КоА).
Эхокардиография показала, что дефекты межжелудочковой перегородки (ДМЖП) перимембранозного типа часто сосуществуют, и субаортальный стеноз является потенциальным долгосрочным последствием хирургического закрытия, которое считается вторичным по отношению к скоплению фиброзной ткани в местах турбулентного потока в выносящем тракте левого желудочка (ВТЛЖ). Другие хирургические вмешательства, связанные с развитием САС, включают коррекцию порока двойного отхождения магистральных сосудов от правого желудочка (ДОСМ) с созданием левого желудочка, ведущего к туннелю аорты, и восстановление дефектов атриовентрикулярного канала (АВК).
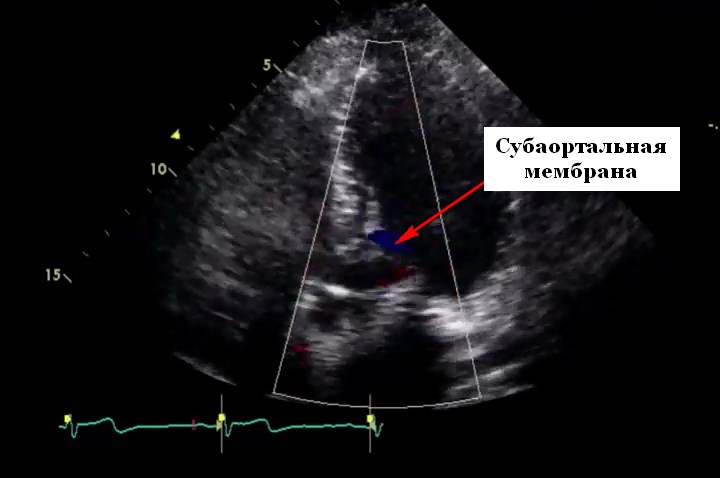
Хирургическая резекция является методом выбора при САС и рекомендуется пациентам с расчетным пиковым градиентом давления (ПКД)> 50 мм рт.ст. или средним градиентом 30 мм рт.ст. и более. Хирургическое вмешательство следует рассматривать у пациентов с более низким расчетным градиентом, если имеется систолическая дисфункция левого желудочка (ЛЖ), дилатация ЛЖ (систолический диаметр> 50 мм) или умеренная / тяжелая аортальная регургитация (АР). Развитие симптомов, связанных с САС (стенокардия, одышка или обморок / предобморочное состояние) при физической нагрузке или сразу после нее, требует хирургического вмешательства. Хирургическое лечение заключается в иссечении мембраны в зоне очагового САС с фокальной миомиэктомией перегородки. Субаортальный стеноз туннельного типа часто требует обширной миомиэктомии или применения процедуры Конно-Растана для реконструкции ВТЛЖ. Операция на АК может потребоваться при наличии умеренной или тяжелой АР. Частота рецидивов САС после хирургического вмешательства наиболее высока в поражениях туннельного типа (37%) и менее распространена при дискретных поражениях (15%). Пациенты, которые имели предоперационный средний допплеровский градиент давления в покое> 40 мм рт.ст. и немедленный послеоперационный градиент> 10 мм рт. подвержены повышенному риску рецидива САС. Время до повторения сужения зависит от типа САС, поражения туннельного типа рецидивируют раньше, чем дискретные поражения. Транскатетерная баллонная дилатация возможна и эффективна для облегчения обструкции у пациентов с тонкими и дискретными перепончатыми САС, частота рецидивов составляет около 20%, что соответствует хирургическому результату.
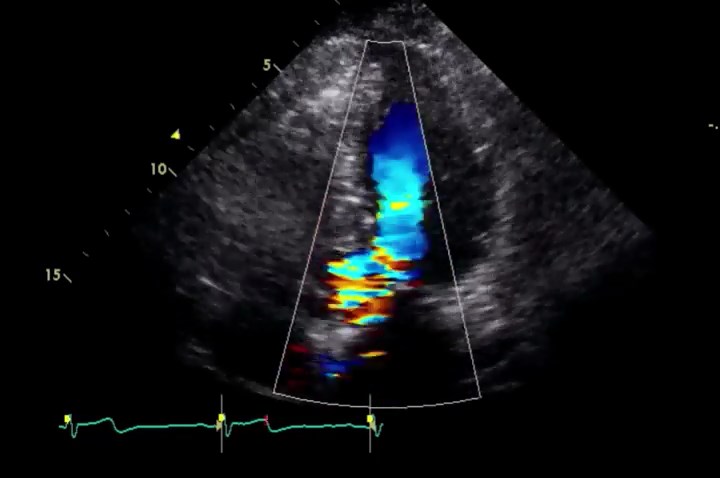
Трансторакальная эхокардиографическая оценка САС должна выполняться комплексно и поэтапно. Стандартные парастернальные, апикальные, подреберные и супрастернальные позиции должны использоваться для двухмерной (2D) и допплеровской оценки. Субаортальный стеноз часто лучше всего визуализируется в парастернальной позиции по длинной оси. Следует осмотреть выносящий тракт ЛЖ, чтобы надлежащим образом идентифицировать расположение мембраны и ДАК. Рекомендуется трехмерная (3D) трансторакальная (TTЭхоКГ) и чреспищеводная (ЧПЭХоКГ) оценка, которая предоставляет дополнительную ценную информацию о типе САС, степени анатомической обструкции (может использоваться для оценки площади отверстия) и наличии других аномалии, такие как ДМЖП или ДАК. Определение типа САС обязательно для правильного отбора пациентов при планировании операции. Пациенты с тонкими и дискретными мембранами могут считаться кандидатами на транскатетерную баллонную дилатацию в месте сужения, тогда как пациенты с более сложным САС (например, диффузным туннельным типом или прикреплением митральных хорд к перегородке) потребуют хирургического вмешательства. Эхокардиография в парастернальной позиции по длинной оси с цветным допплером демонстрирует ускорение потока в ВТЛЖ и может использоваться для оценки наличия ДМЖП. Непрерывно-волновая допплеровская оценка наиболее точно выполняется с апикальной, супрастернальной или субкостальной позиции. Полученный методом непрерывноволнового допплеровского анализ пиковый градиент давления> 50 мм рт.ст. или средний градиент давления> 30 мм рт.ст. считается тяжелым и предвещает плохой прогноз, если его не лечить.
Прогрессирующая регургитация на аортальном клапане и, реже, его стеноз могут быть результатом повреждения, вызванного турбулентным систолическим потоком от САС, даже при отсутствии ДАК. Трудно установить степень последовательной обструкции с помощью допплера у пациентов с САС и стенозом АК, однако 2D и 3D оценка морфологии и движения AК полезна для определения степени обструкции клапанов. Первичный гемодинамический эффект на левый желудочек заключается в увеличении постнагрузки с результирующей гипертрофией и снижением диастолической податливости. Степень САС может быть недооценена из-за градиента давления, полученного из скорости, при наличии подавленной систолической функции ЛЖ или не ограничивающего ДМЖП, который позволяет шунтировать в легочную артериальную циркуляцию слева направо.
