С чего начать обследование сердца
УЗИ сердца при оценке болевого синдрома в грудной клетке
При возникновении дискомфорта или болей в сердце встает вопрос о том, с чего начать обследование сердца? Не все пациенты с длительной болью в груди вследствие ишемии миокарда или инфаркта присутствующих с типичными изменениями на ЭКГ. Более 50% больных инфарктом миокарда при обследовании имеют неспецифические симптомы на ЭКГ. Быстрое количественное определение изоферментов креатинкиназы (CK-МВ) надежен в обнаружении инфаркта миокарда в течение первых 6 часов после начала боли в груди (впрочем, чувствительность КФК-МВ изофермента анализы не могут быть удовлетворительными, если анализ осуществляется в течение 4 часов после появления боли за грудиной. Тропонин Т и тропонин I является более чувствительным маркерам некроза ткани миокарда. Еще совсем недавно плазменный миелопероксидазы лейкоцитарной фермента, был найден для прогнозирования риска инфаркта миокарда в отделении неотложной помощи с болью в груди. Уровень миелопероксидазы возрастает в виновником поражения, которые имеют трещины или разрыва у пациентов с внезапной смерти от сердечных причин. Кроме того, повышенный уровень миелопероксидазы независимо друг от друга предсказали больших кардиальных событий в последующие 1-месячного и 6-месячного периодов.
В клинической оценке боли в грудной клетке электрокардиография является существенным дополнением к истории болезни и физическому осмотру. Быстрый и точный диагноз у пациентов с острым инфарктом миокарда жизненно важен, так как ускоренная реперфузионная терапия может улучшить прогноз. Наиболее часто используемым электрокардиографическим критерием для выявления острого инфаркта миокарда является повышение сегмента ST в двух или более анатомически смежных отведениях. Высота сегмента ST, связанная с развивающимся инфарктом миокарда, часто легко идентифицируется, но знание общих «псевдо» инфарктных структур имеет важное значение, чтобы избежать ненужного использования тромболитической терапии.
На ранних стадиях острого инфаркта миокарда электрокардиограмма может быть нормальной или почти нормальной. Менее половины пациентов с острым инфарктом миокарда имеют четкие диагностические изменения на своем первом обследовании. Около 10% пациентов с подтвержденным острым инфарктом миокарда (на основе клинической истории и ферментативных маркеров) не имеют развития сегмента ST или депрессии. В большинстве случаев, однако, серийные электрокардиограммы показывают эволюционные изменения, которые, как правило, следуют хорошо распознанным критериям.

Среди основных преимуществ эхокардиографии является то, что она может быть выполнена в отделении неотложной помощи и ее результаты доступны сразу. Как уже упоминалось, сократимость миокарда, уменьшает или прекращает сразу же после ишемия или инфаркт и проявляется как нарушение локального сокращения стенок миокарда, что у большинства пациентов, это легко определить на эхокардиографии. Таким образом, использование метода выявления зон гипокинеза как маркер инфаркта миокарда у пациентов с длительной болью в груди с оценкой их на эхокардиографии и снятии ЭКГ привлекательна. Отсутствие аномалий движения стенки ЛЖ, как правило, исключает наличие ишемии миокарда.
Кроме того, несмотря на наличие нарушений локальной сократимости на УЗИ сердца обладает высокой чувствительностью для выявления инфаркта миокарда, положительная прогностическая ценность составляет около 30%, потому что сами зоны не являются специфичными для острого инфаркта миокарда и некоторых больных нестабильной стенокардией без поражения миокарда. Однако, эхокардиография может быть полезным и экономически эффективным, если пациенты имеют низкий до среднего уровня риск развития острого инфаркта миокарда.
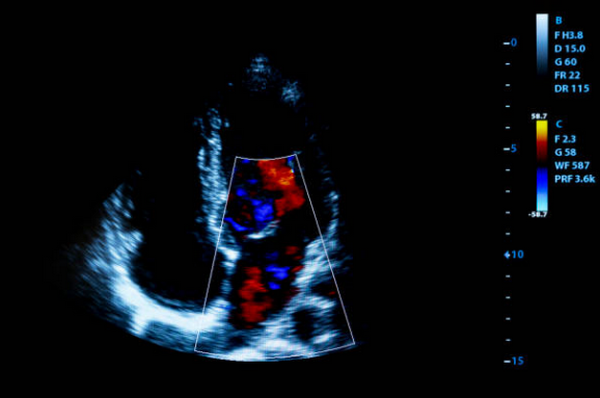
Иногда, эхокардиография может быть полезной в выявлении потенциально фатальной причиной синдрома боли в грудной клетке, таких как тромбоэмболия легочной артерии, расслоение аорты или тампонада сердца. Частота этих находок мало, но без антикоагулянтной или тромболитической терапии у некоторых из этих пациентов могут иметь катастрофические клинические исходы. Подход, описанный здесь, требует, чтобы проведение эхокардиографии было проведено как можно оперативно. УЗИ сердца можно сделать в динамике и интерпретированы в отдаленные сроки с использованием цифровой эхокардиографии, но для этого надо иметь соответствующую подготовку персонала для выполнения экстренной эхокардиографии.
Эхокардиографический анализ нарушения локальной сократимости полезен диагностически и клинически даже у пациентов с классическими болями в груди и подъем сегмента ST на ЭКГ. Сумма зон поражения миокарда на риск может быть оценен путем расчета. Если он больше, чем 1.7, то это как правило, предполагает дефект перфузии более чем на 20% и увеличению числа осложнений, если аномалий движения стенки сочетаются с дальнейшей реперфузионной терапией. Через несколько дней после реперфузионной терапии, региональный анализ движения стенок может быть полезен на УЗИ сердца при оценке функционального восстановления, хотя перфузионная эхокардиография с контрастированием миокарда может предсказать функциональное восстановление только после реперфузионной терапии. Также двухфазные реакции во время нагрузочной эхокардиографии в ранние сроки после инфаркта миокарда прогнозирует жизнеспособности миокарда.
Объема миокарда в зоне риска из пораженной артерии также может определить при обследовании сердца на УЗИ, такие пациенты получат наибольшую пользу от острой инвазивной терапии. Пациенты с большим объемом поражения миокарда в группе риска (как правило, передней стенки инфаркт миокарда) извлечет больше пользы от реперфузионной терапии, чем те, которые имеют небольшое количество поврежденного миокарда и имеющие меньший риск. Когда пациент имеет при обследовании на ЭКГ инфаркт миокарда с подъемом сегмента ST, пораженный миокард на эхокардиографии акинетический или дискинетический. После успешной реперфузии миокарда в течение соответствующего времени (обычно в течение 4 часов), он восстанавливается и имеет больше нормально сократительных зон при последующих исследованиях на эхокардиографии. Острый инфаркт миокарда может быть остановлен в подгруппе пациентов при кратковременной ишемической атаке. Серийные эхокардиографические исследования показали, что улучшение региональной сократимости миокарда проявляется в течение от 24 до 48 часов и что улучшение продолжается в течение нескольких дней до месяцев. Таким образом, последующие проведённые УЗИ сердца полезны в обнаружении реперфузированных сегментов миокарда и расширение инфаркта.
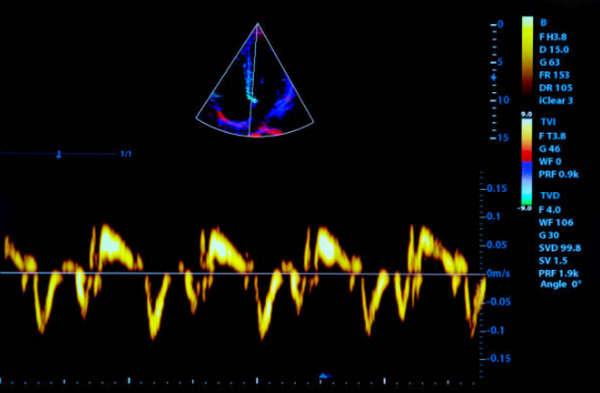
Постоянные зоны акинеза не всегда свидетельствует о неудачной реперфузии. Когда миокард остается акинетическим, будучи жизнеспособным, низкие дозы добутамина или контрастной эхокардиографии могут быть полезными в демонстрации его жизнеспособности. Увеличение или ремоделирование ЛЖ, один из самых сильных предикторов кардиальных событий после инфаркта миокарда при обследовании сердца, который легко оценить на серийной ЭхоКГ и может быть предсказано отсутствие перфузии миокарда.
Измерения деформации используется для выявления острой ишемии миокарда. В исследовании пациентов, перенесших плановую коронарную ангиопластика, систолический стрейн был сокращен и постсистолическим увеличена, но с задержкой. Расслабление ишемизированных сегментов миокарда нарушается, как следствие, физиологическое раннее диастолическое истончение и удлинение сменяются постоянным постсистолическим утолщением и укорочением. Поэтому, возможно, что аномальные региональных деформации (например, снижение систолической деформации) и скорости деформации может быть использован в качестве маркера острой ишемии, если изменение напряжения или локальные деформации могут быть визуализированы или легко определяться на эхокардиографии.
Обследования сердца при остром инфаркте миокарда
Во многих учебных заведениях мира, первичное чрескожное коронарное вмешательство (ЧКВ) является методом выбора для лечения острого инфаркта миокарда и смертность после острого инфаркта миокарда значительно снизилась. Роль эхокардиографии вписалась в стратегию лечения острого инфаркта миокарда и в настоящий момент она изменилась. Свои нынешние роли могут УЗИ сердца могут быть классифицированы следующим образом:
- Постановка диагноза и исключения острого инфаркта миокарда у пациентов с длительной болью в груди и неоднозначными данными ЭКГ,
- Оценка объема миокарда в зоне риска ишемии и установление окончательного размера инфаркта после реперфузионной терапии,
- Оценка нестабильной гемодинамики сердца,
- Выявление осложнений инфаркта,
- Оценка жизнеспособности миокарда и
- Стратификация риска.
Таким образом, на различных этапах развития острого инфаркта миокарда, эхокардиография имеет важное значение в обеспечении анатомических, функциональных и гемодинамических информации.
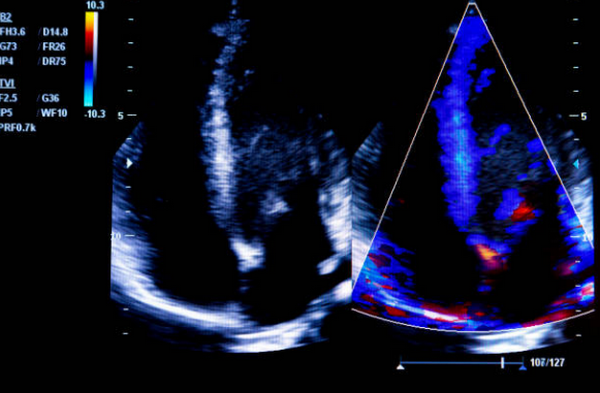
Механические осложнения кардиогенный шок при эхокардиографическом исследовании
Известно, что у пациенты, с кардиогенным шоком после инфаркта миокарда, имеют плохой прогноз. Однако, если причина является обратимой, то это имеет огромное клиническое значение для скорейшего определения основной причины и правильное лечение может быть значительно улучшить состояние пациента. В исследовании, когда причиной ухудшения работы сердца был кардиогенный шок после инфаркта миокарда, остановка сердца встречалась в 85% случаях, механические осложнения в 8%, инфаркт миокарда правого желудочка (ПЖ) в 2%, и другие коморбидные состояния в 5%. Двухмерная и допплер-эхокардиография с цветным допплеровским картированием используются для оперативного выявления причины у этих пациентов, особенно при проверке механических осложнений. Эхокардиография, проведенная вскоре после острого инфаркта миокарда с кардиогенным шоком, показала, что степень выраженности митральной недостаточности и фракция выброса ЛЖ (ФВ ЛЖ) были единственными независимыми предикторами выживаемости. Кроме того, чреспищеводное УЗИ сердца должно быть выполнена незамедлительно у пациентов, у которых изображение в области сердца при трансторакальной эхокардиографии может оказаться невозможным или если изображения, полученные в интенсивной терапии, не являются оптимальными. Наличие ненормальной систолической функции в критическом состоянии или у гемодинамически нестабильных пациентов должна немедленно вызвать подозрение механическое осложнение.
