Эхокардиография и источники эмболии (часть 1)
Эхокардиографию (ЭхоКГ) нам приходится проводить для поиска причин эмболии в сосуды. Острая ишемия органа или конечности из-за артериальной непроходимости обычно возникает из-за одного из двух патогенных процессов: острой тромботической окклюзии на субстрате значительного местного артериального заболевания (чаще всего атеросклероз) или эмболии из полостей сердца или проксимальных пораженных крупных сосудов (чаще всего грудной аорты). Доля острых ишемических событий, имеющих эмболическую этиологию, зависит от ряда факторов, включая возраст пациента, вероятность внутреннего сосудистого заболевания и пораженное сосудистое русло. Исследование после такого события сосредоточено на определении основного процесса, ответственного за событие, с основной целью предотвратить дальнейшие потенциально более разрушительные события. Эхокардиография — это основной диагностический инструмент для выявления потенциального источника эмболии. В оставшейся части этого обсуждения источники эмболов внутри сердца и грудной аорты будут вместе обозначаться как «сердечно-сосудистые эмболы», подчеркивая, что не все потенциальные источники эмболов находятся в сердце. Это часть блога изначально фокусируется на определении роли эхокардиографии в оценке потенциальных сердечно-сосудистых источников эмболии, включая показания для ЭхоКГ, которая является оптимальным методом (чреспищеводный или трансторакальный), и как выполнить комплексное эхокардиографическое исследование. В оставшейся части обсуждаются отдельные потенциальные источники (как вероятные, так и возможные), рассматриваются доказательства связи между каждым потенциальным источником и эмболическими событиями, характерные эхокардиографические особенности, как всесторонне оценивать их с помощью эхокардиографии и текущие стратегии лечения.
Эпидемиология сердечно-сосудистой эмболии
Инсульт - одно из наиболее частых и разрушительных клинических последствий сердечно-сосудистой эмболии. В 2009 году стандартизованный по возрасту коэффициент смертности от всех ССЗ составлял 237,1 на 100 000 человек, а уровень смертности от инсульта, заболеваний сердца и других сердечно-сосудистых причин составил 38,9, 116,1 и 81,0 на 100 000, соответственно. Кроме того, данные NHANES за 2009–2010 гг. Показывают, что в целом 7,2% пациентов сами сообщили о наличии какого-либо типа ССЗ, включая 3,2% с ишемической болезнью сердца (ИБС), 2,7% с инсультом и 2,0% с застойной (хронической) сердечной недостаточностью (ХСН). В настоящее время предполагается, что около 20% острых неврологических событий связаны с сердечно-сосудистыми эмболами. Еще 40% классифицируются как «криптогенные», хотя появляется все больше данных, предполагающих связь с возможными сердечно-сосудистыми источниками эмболов в них. У молодых людей с острым ишемическим инсультом (до 45 лет) доля сердечно-сосудистой эмболии значительно выше (> 50%), поскольку потенциальный источник эмболии, скорее всего, будет единственной идентифицируемой причиной. Это контрастирует с пациентами старшего возраста, которые с большей вероятностью имеют идентифицируемое сопутствующее врожденное цереброваскулярное заболевание. Также возможно, что у некоторых пациентов весь источник эмбола мог мигрировать в сосудистое русло, создавая ложноотрицательное эхокардиографическое исследование, недооценивая истинную долю пациентов, у которых есть сердечно-сосудистый источник эмболии.
Возможные сердечно-сосудистые источники эмболии
Литература, документирующая взаимосвязь между потенциальными источниками сердечно-сосудистой эмболии, ограничена тем фактом, что большая часть текущих данных основана на нерандомизированных сериях случай-контроль, а не на проспективных исследованиях. Потенциальные источники эмболов в сердечно-сосудистой системе лучше всего разделить на две группы в зависимости от уровня имеющихся в настоящее время доказательств: вероятные или возможные источники (таблица 1). Большинство из них происходит из-за эмболии внутрисердечного тромба, который в более чем половине всех случаев локализуется в пределах левого предсердия (ЛП), прежде всего в пределах ушка левого предсердия (УЛП). Фибрилляция предсердий и ревматическая болезнь митрального клапана (в первую очередь митральный стеноз) являются наиболее частыми предрасполагающими факторами. Тромб левого желудочка (ЛЖ), обычно возникающий в условиях серьезной аномалии движения апикальной стенки (акинезия или аневризма), является вторым наиболее частым потенциальным источником эмболии (25%). Большие вегетации и левосторонние опухоли (миксома или папиллярная фиброэластома) встречаются гораздо реже. Все чаще на эхокардиографии выявляется атерома грудного отдела аорты, которая связывается с эмболическими событиями. Эта связь наиболее высока для «сложных» бляшек (например, толщиной> 4 мм или поражений на ножке и подвижных тромботических наложений). Острое ишемическое событие у пациента с протезом механического клапана является кардиоэмболическим, пока не будет доказано обратное.
Другие результаты эхокардиографии перечислены как возможные источники, поскольку уровень доказательности менее надежен. Открытое овальное окно (ООO) связано с повышенным риском ишемического инсульта, особенно у молодых людей, хотя это настолько частое явление в общей популяции (20–25%), что определение точной причины и следствия затруднено. Комбинация аневризмы межпредсердной перегородки (AМПП) и ООО связана с многократным увеличением риска инсульта по сравнению с одним открытым овальным окном. Другие находки, предполагающие возможные ассоциации с эмболическими событиями, включают спонтанный эхоконтрастирование (СЭК) в левом предсердии, клапанный фиброз, кальцификацию митрального кольца, пролапс митрального клапана и более мелкие вегетации.
Рекомендации по эхокардиографии у пациентов с неврологическими нарушениями или другими сосудистыми эмбологенными событиями (обновление рекомендаций AHA / ACC / ASE 2003 по клиническому применению эхокардиографии)
I класс.
- Пациенты любого возраста с резкой окклюзией основной периферической или висцеральной артерии
- Более молодые пациенты (обычно <45 лет) с цереброваскулярными нарушениями
- Пожилые пациенты (обычно> 45 лет) с неврологическими нарушениями без признаков цереброваскулярного заболевания или другой очевидной причины
- Пациенты, для которых клиническое терапевтическое решение (например, антикоагулянтная терапия) будет зависеть от результатов эхокардиографии.
Класс IIa
- Пациенты с подозрением на эмболию и цереброваскулярные заболевания сомнительной значимости
Класс IIb
- Пациенты с неврологическими нарушениями и внутренними цереброваскулярными заболеваниями, природа которых достаточна, чтобы вызвать клиническое событие.
III класс
- Пациенты, для которых результаты эхокардиографии не повлияют на решение о назначении антикоагулянтной терапии или иным образом не повлияют на подход к диагностике или лечению.
Трансторакальная и чреспищеводная эхокардиография для выявления причины эмболии
Чувствительность трансторакальной эхокардиографии (TTЭхоКГ) для обнаружения потенциальных источников эмбола низкая, так как наиболее частые потенциальные причины плохо визуализируются с помощью этой методики. При отсутствии клинических сердечных заболеваний диагностическая ценность составляет всего 1%, а с клиническими сердечными аномалиями увеличивается до 15%. Его основное применение - оценка глобальной и региональной систолической функции ЛЖ и апикального тромба в левом желудочке.
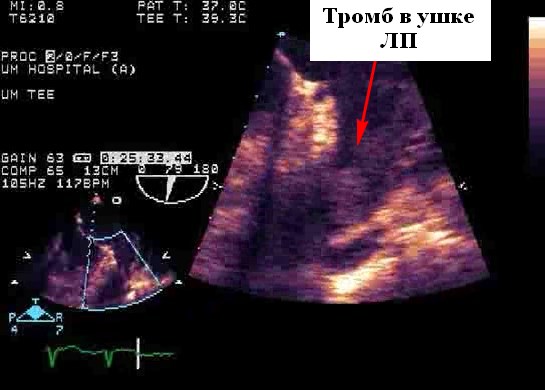
Оценка межпредсердной перегородки и грудной аорты. В целом чреспищеводная эхокардиография (ЧПЭХоКГ) выявляет значительно больше потенциальных источников эмболии, чем TТЭхоКГ (39–57% против 15–19%). Оценка потенциального источника эмбола в настоящее время является основным клиническим показанием для ЧПЭХоКГ в большинстве лечебных учреждений (26%). Использование контраста могло бы повысить эффективность ЧПЭхоКГ для обнаружения тромбов в ушке левого предсердия, и польза была максимальной, когда исследования были ограничены наличием спонтанного эхо-контрастирования или когда была низкая скорость опорожнения ушка левого предсердия. Кроме того, контраст часто помогает отличить плотный спонтанный эхоконтрастный осадок и необходим для оптимальной визуализации ЛП и тромба, в частности, расположенной сзади ушка левого предсердия (наиболее частое место расположения тромба). Однако, вероятно, лучше рассматривать эти два метода как взаимодополняющие, а не исключающие друг друга.
