УЗИ узлов щитовидной железы (окончание)
Системы, используемые для стратификации риска злокачественности в узле щитовидной железы по УЗИ, были основаны на описании отдельных ультразвуковых особенностей или различных систем оценки, которые учитывают паттерны или количество подозрительных ультразвуковых особенностей. В соответствии с рекомендациями 2005 года, биопсия с критериями ограничения по размеру зависит от индивидуальных особенностей, выявленных на УЗИ. Недавний метаанализ, изучающий прогностическую ценность отдельных особенностей на ультразвуковом исследовании с использованием комбинированных данных, показал, что наивысший коэффициент вероятности для злокачественности (ДИ 6,6–18,9) был получен у узлов с более высокой, чем широкой характеристикой (высота больше ширины). Другими индивидуальными прогностическими признаками были инфильтративные поля, внутренние кальцификации, гипоэхогенность и солидный узел. Тем не менее, каждый из этих индивидуальных признаков имел относительно скромные отношения правдоподобия, и когда была учтена распространенность рака щитовидной железы, они приводили к относительно скромной вероятности возникновения рака щитовидной железы после тестирования. Другие мета-анализы дали аналогичные выводы. Таким образом, использование одного признака УЗИ не учитывает изменение риска, которое может происходить с комбинацией функций, а также не учитывает отдельные факторы риска пациента.
Комбинации или паттерны особенностей УЗИ имеют более высокую прогностическую ценность для рака щитовидной железы по сравнению с индивидуальными особенностями. Американская ассоциация щитовидной железы (ATA) разработала критерии для оценки риска злокачественности в узле, используя образец сонографических особенностей. При использовании этой системы солидный гипоэхогенный узелок, который также имеет нерегулярные края, микрокальцификации, более высокую, чем широкую форму, экструзивный компонент мягких тканей или быстрое увеличение объема щитовидной железы, считается высоким подозрением и имеет по меньшей мере 70– 90% риск малигнизации.
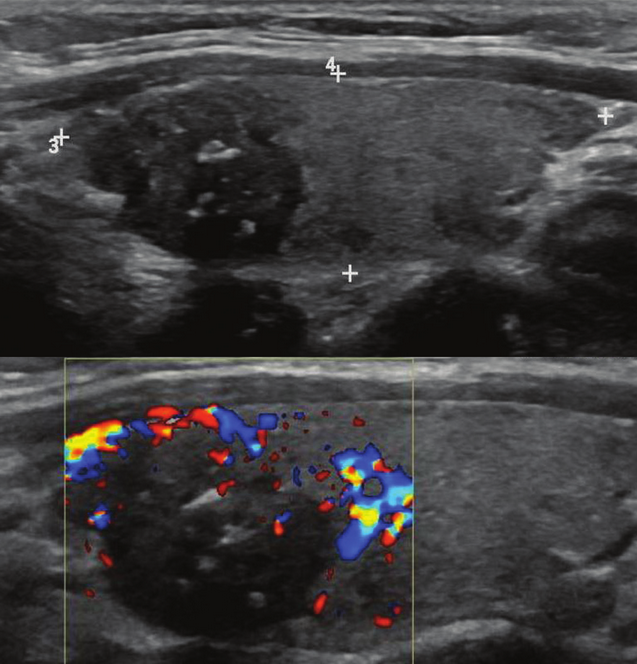
На рисунке показан узел с сонографическими признаками АТА высокого риска, который при биопсии оказался папиллярным раком щитовидной железы.
Солидные гипоэхогенные узлы без этих дополнительных признаков считаются промежуточным риском с риском развития злокачественных опухолей 10–20%. Изоэхогенные или гиперэхогенные узлы без этих признаков имеют низкий риск (5–10%) злокачественности. Гиперэхогенный узел признаками низкого риска показан на рисунке ниже.
Губчатые узлы имеют очень низкий (<3%) риск злокачественности, тогда как чисто кистозные поражения считаются доброкачественными с <1% риском злокачественности. На основании этих различных оценок риска рака щитовидной железы, ATA предлагает различные критерии размера для принятия решения о проведении тонкоигольной аспирационной биопсии. Например, узлы с сонографическими картинами высокого и промежуточного риска рекомендуются для биопсии, если они имеют размер более 1 см, тогда как узлы низкого риска рекомендуются для биопсии, если они имеют размер более 1,5 см.
Было разработано несколько других систем для оценки риска злокачественных образований щитовидной железы. Некоторые из них являются количественными и основаны на подсчете количества подозрительных функций по УЗИ и формировании оценки риска. С тех пор системы отчетности и обработки изображений щитовидной железы (TIRADS), впервые сформулированные в 2009 году, были предложены во многих различных итерациях. Значимость сонографических признаков и комбинаций признаков сходна со схемой ATA, но предельные размеры для тонкой аспирации иглы и потребность в последующей сонографии немного отличаются.
Узлы щитовидной железы также могут быть оценены с использованием тензометрической эластографии, которые имеются в датчиках УЗИ и применяются для сжатия и декомпресии исследуемого узла (узлов) щитовидной железы. Изменение сигнала измеряет жесткость ткани, которая обычно отображается в виде непрерывного набора цветов. Чем больше жесткость ткани щитовидной железы, тем больше вероятность злокачественности. Однако в настоящее время этот метод не был достаточно стандартизирован для общего использования. Компьютерные диагностические системы также были изучены для оценки узлов щитовидной железы. Хотя этот тип искусственного интеллекта в настоящее время не работает лучше, чем опытный врач УЗИ, производя подобную чувствительность, но меньшую специфичность и точность, такие алгоритмы могут быть усовершенствованы в будущем.
Сонографические паттерны могут также использоваться для наблюдения за узлами щитовидной железы, у которых после биопсии обнаружена доброкачественная цитология. Если узел имеет высокую степень подозрений на УЗИ, то назначается последующее ультразвуковое исследование и биопсия в течение 12 месяцев. Узлы с паттернами среднего или низкого риска заслуживают повторного обследования на УЗИ через 12–24 месяца и повторной биопсии, если появляются новые подозрительные сонографические признаки или рост. Доброкачественные узлы с очень низким уровнем подозрительности могут не требовать сонографического наблюдения или могут быть повторно обследованы через 24 месяца.
Лимфатические узлы на УЗИ при узлах щитовидной железы
УЗИ также имеет большое значение для выявления аномальных шейных лимфатических узлов у лиц, которые оцениваются для возможного диагноза рака щитовидной железы, для тех, кто проходит оценку до операции на щитовидной железе по поводу известного рака щитовидной железы, и для наблюдения за щитовидной железой и шеей у пациентов после операции по поводу рака щитовидной железы. Доброкачественные лимфатические узлы обычно имеют овальную форму с сохраненными воротами, в то время как лимфатические узлы, содержащие метастатический рак щитовидной железы, чаще имеют округлую форму, потерю жирового просвета, кистозные изменения, микрокальцификации или нерегулярную внутреннюю гиперваскулярность.
